Therapie der generalisierten Myasthenia gravis
Die generalisierte Myasthenia gravis ist zwar nicht heilbar, die Symptome können jedoch durch eine Behandlung gelindert werden. Für die Therapie der generalisierten Myasthenia gravis stehen unterschiedliche Behandlungsmöglichkeiten zur Verfügung:1
Medikamente1
- Acetylcholinesterase-Hemmer verlangsamen den Abbau des Botenstoffs Acetylcholin (ACh), der eine wichtige Rolle in der Kommunikation zwischen Muskel und Nerv spielt.
- Immunsuppressive Medikamente hemmen die Produktion von schädlichen Autoantikörpern wie z. B. Antikörpern gegen Immunglobulin G (IgG)-Proteine.
- Monoklonale Antikörper werden in der Regel als Infusion verabreicht und können helfen, bestimmte Bereiche des Immunsystems zu kontrollieren.
Operation1
- Bei einer Thymektomie wird die Thymusdrüse entfernt. Diese Operation kann dazu beitragen, die Erkrankung zu kontrollieren. Bei Menschen mit generalisierter Myasthenia gravis ist die Thymusdrüse oft verändert bzw. vergrößert.
Notfallbehandlung im Krankenhaus bei myasthener Krise1
- Bei einer myasthenen Krise kann ein Plasmaaustausch durchgeführt werden. Dabei werden schädliche Autoantikörper aus dem Blutplasma entfernt.
- Eine weitere Behandlungsoption bei einer myasthenen Krise ist intravenöses Immunglobulin. Dabei werden normale Antikörper, die das Immunsystem unterstützen, injiziert.
Wie wirkt VYVGART (Efgartigimod alfa)?
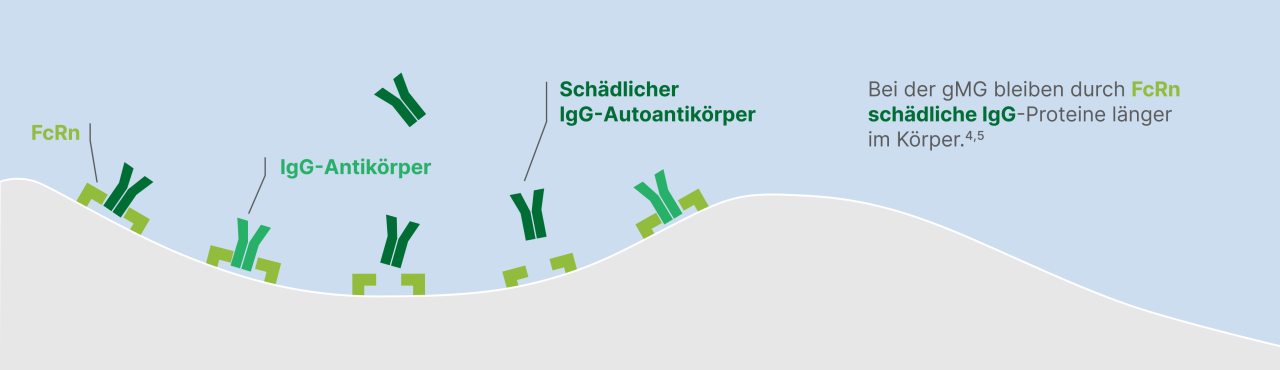
IgG-Antikörper als wichtiger Bestandteil des Immunsystems schützen den Körper normalerweise vor Infektionen und anderen Krankheiten. Bei der generalisierten Myasthenia gravis bildet das Immunsystem irrtümlicherweise auch schädlichen IgG-Antikörper, die die Kommunikation zwischen Nerven und Muskeln stören.2 Diese schädlichen Antikörper werden auch Autoantikörper genannt. Antikörper wie IgG-Proteine binden im Körper an ein Protein namens neonataler Fc-Rezeptor (FcRn).3 Die Aufgabe dieser FcRn ist es, IgG-Antikörper vor dem körpereigenen Abbau zu schützen und sie dadurch dem Körper zur Wiederverwendung bereitzustellen (Recycling). Der Vorteil ist dabei, dass der Körper nicht ständig zu große Mengen an IgG-Antikörpern nachbilden muss. Der Nachteil ist allerdings, dass dadurch ebenso schädliche bzw. autoimmun wirksame IgG-Antikörper, wie sie auch bei Menschen mit generalisierter Myasthenia gravis vorliegen, länger im Körper verweilen.
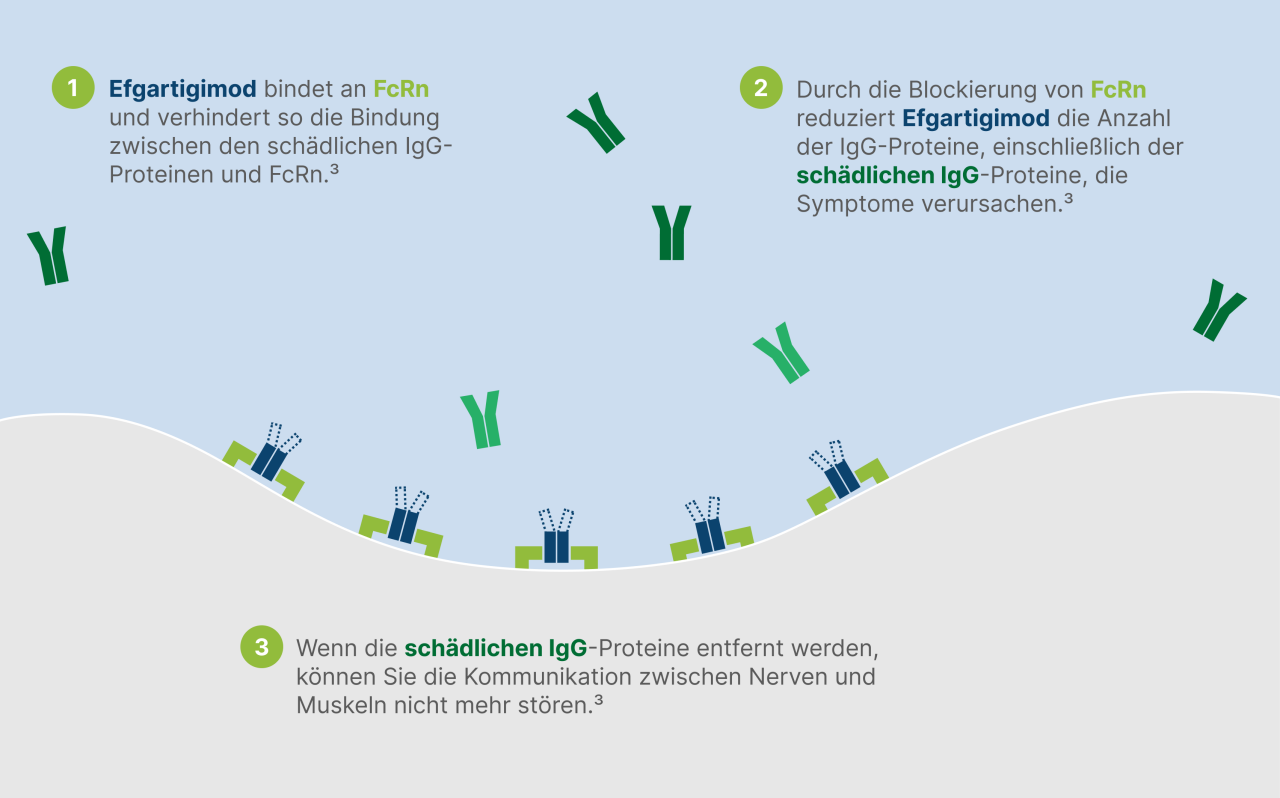
VYVGART enthält den Wirkstoff Efgartigimod alfa, der aufgrund seiner Struktur ebenfalls an den neonatalen Fc-Rezeptor (FcRn) binden kann. Dadurch wird das körpereigene Recycling von IgG-Antikörpern in einem bestimmten Ausmaß verringert und resultiert so auch in einem schnelleren Abbau der schädlichen IgG-Antikörper.
Im Video erfährst Du unter anderem, wie deine Muskeln arbeiten, wie die Anti-AChR-Antikörper-positive generalisierte Myasthenia gravis entsteht und wie deine Therapie mit VYVGART funktioniert.
Video: generalisierte Myasthenia gravis im Fokus
DE-VYV-23-00025
Wie läuft die Behandlung mit VYVGART (Efgartigimod alfa) ab?
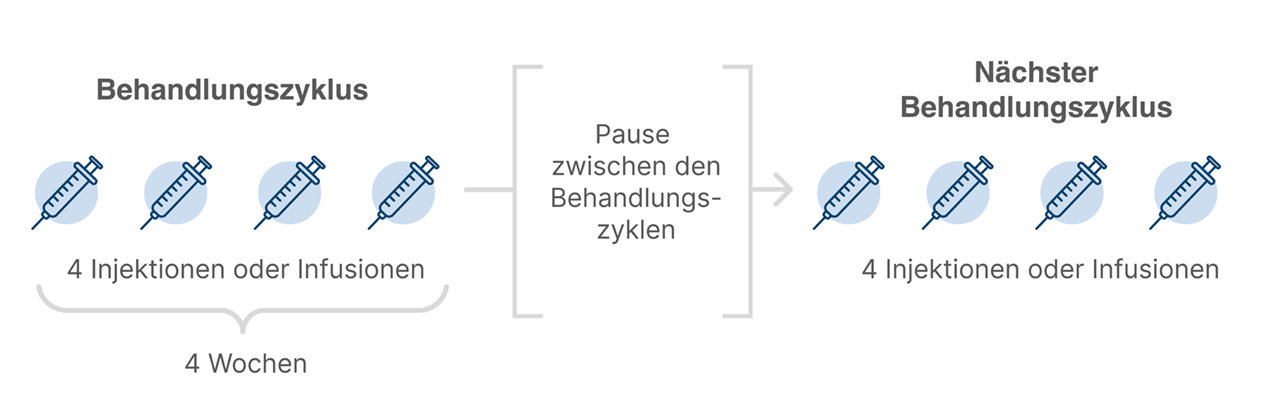
VYVGART (Efgartigimod alfa) ist in verschiedenen Verabreichungsformen erhältlich: Seit kurzem steht das Arzneimittel als Fertigspritze zur Selbstverabreichung unter die Haut (subkutan, s.c.) zur Verfügung.4,* Darüber hinaus ist VYVGART als ebenfalls s.c. Injektionslösung mittels eines geflügelten Infusionssets oder als intravenöse (i.v.) Infusion erhältlich. Ein Behandlungszyklus besteht bei allen Verabreichungsformen jeweils aus einer Injektion oder Infusion pro Woche. Insgesamt werden pro Behandlungszyklus jeweils 4 Injektionen oder Infusionen gegeben.4,5,6
Nach dem ersten Behandlungszyklus beurteilt dein:e Ärzt:in, wann du weitere Behandlungszyklen benötigst.
Sprich deine:n Ärzt:in am besten direkt am Anfang der Therapie darauf an, wann der nächste Therapiezyklus begonnen werden soll. Die Therapie wird individuell auf dich abgestimmt und richtet sich nach deinem persönlichen Ansprechen. Zu Beginn können feste Intervalle für die Behandlungszyklen erforderlich sein, bevor im weiteren Verlauf eine an deine Bedürfnisse angepasste Verabreichung erfolgen kann. Wichtig für die Beurteilung sind:
- - Die Ausprägung und Stärke deiner Symptome (meist werden sie mit dem MG-ADL-Fragebogen bewertet)
- - Dein Ansprechen auf die Behandlung
Selbstverabreichung der VYVGART s.c. Fertigspritze
Die VYVGART s.c. Fertigspritze kannst du unter bestimmten Umständen selbst oder deine Pflegeperson verabreichen. Dabei sind in jedem Fall folgende Punkte zu beachten:4
- Die Injektion der VYVGART s.c. Fertigspritze muss im ersten Behandlungszyklus und bei der ersten Anwendung im zweiten Behandlungszyklus entweder von einer:m Ärzt:in oder unter ärztlicher Aufsicht durchgeführt werden. Ab der 6. Injektion kannst du oder deine Pflegeperson die Injektion selbständig durchführen.
- Die Injektion darf nur nach vorheriger, ausreichender Schulung durch deine:n Ärzt:in selbstständig angewendet werden. Dein:e Ärzt:in muss dir oder der verabreichenden Pflegeperson gezeigt haben, wie die Injektion richtig vorbereitet und die Injektionslösung richtig injiziert wird.
- Die VYVGART s.c. Fertigspritze darf nur s.c. (unter die Haut) angewendet werden.
- Die VYVGART s.c. Fertigspritze ist nur zur einmaligen Anwendung bestimmt und kann nicht wiederverwendet werden.
Ausführliche Hinweise zur Injektion des Arzneimittels sind dem Abschnitt „Wichtige Hinweise zur Anwendung” in der Packungsbeilage zu entnehmen. Lies daher vor Anwendung sorgfältig die Packungsbeilage durch.
Was ist in einer Packung der VYVGART s.c. Fertigspritze enthalten?
Eine Packung enthält eine Fertigspritze.
Zusätzliche Materialien, die du für die Anwendung benötigst, die nicht in der Packung der VYVGART Fertigspritze enthalten sind:
- 1 Nadel mit Schutzvorrichtung 25 G, 16 mm Länge
- 1 Alkoholtupfer
- 1 Behälter für spitze/scharfe Gegenstände
- 1 sterile Mullkompresse und/oder Pflaster (nach Bedarf)
Selbstverabreichung der VYVGART s.c. Injektionslösung mittels eines geflügelten Infusionssets
Auch die VYVGART s.c. Injektionslösung kann unter bestimmten Umständen von dir selbst oder deiner Pflegeperson verabreicht werden. Dabei sind in jedem Fall folgende Punkte zu beachten:5
- Die VYVGART s.c. Injektionslösung muss im ersten Behandlungszyklus und bei der ersten Anwendung im zweiten Behandlungszyklus entweder von einer:m Ärzt:in oder unter deren:dessen Aufsicht durchgeführt werden.
- Die Injektion darf nur nach vorheriger, ausreichender Schulung durch deine:n Ärzt:in selbstständig angewendet werden. Dein:e Ärzt:in muss dir oder der verabreichenden Pflegeperson gezeigt haben, wie die Injektion s.c. (unter die Haut) richtig vorbereitet und die Injektionslösung richtig injiziert wird.
- Die Injektionslösung darf nur s.c., das heißt unter die Haut, angewendet werden.
- Die Durchstechflasche ist nur zum einmaligen Gebrauch bestimmt und muss nach Anwendung entsorgt werden.
Ausführliche Hinweise zur Injektion des Arzneimittels sind dem Abschnitt „Wichtige Hinweise zur Anwendung” in der Packungsbeilage zu entnehmen. Lies daher vor Anwendung sorgfältig die Packungsbeilage durch.
VYVGART® kann als subkutane Injektion auch von Betroffenen und deren Pflegepersonen selbst unter die Haut gespritzt werden. Oft gibt es im Zusammenhang mit der individuellen Anwendung zuhause oder aber auch unterwegs, z.B. auf Reisen, noch einmal Fragen. Dr. med. Frauke Stascheit, Berlin, erklärt im Interview zum Thema „Anwendung von VYVGART® in der Praxis“ die wichtigste Punkte der subkutanen Gabe, gibt praktische Tipps zur Injektion und führt aus, was bei einer Umstellung von der intravenösen Infusion auf die subkutane Injektion zu beachten ist.
DE-ESC-24-00017, Stand Nov 2024
In diesem Video erhältst du einen Überblick zu den wichtigsten Schritten der Anwendung von VYVGART (Efgartigimod alfa) 1.000 mg Injektionslösung in einer Fertigspritze. Bitte beachte, dass das Video nur der Illustration dient. Die detaillierte Beschreibung findest du in der Packungsbeilage.
DE-VYV-25-00043, Stand Apr 2025
Was ist in einer Packung der VYVGART s.c. Injektion enthalten?
Eine Packung der VYVGART s.c. Injektionslösung enthält eine Durchstechflasche. Weitere für die Anwendung erforderliche Materialien sind in der Packung nicht enthalten. Diese können dir verschrieben werden – spreche hierzu deine:n Ärzt:in an.
Was wird zusätzlich zur Verabreichung der VYVGART s.c. Injektion benötigt?
Zusätzliche Materialien, die du für die Anwendung benötigst, die nicht in der Packung der VYVGART s.c. Injektionslösung enthalten sind:
- Alkoholtupfer
- 1 Luer-Lok-Spritze, 10 ml, 0,2-ml-Skalierung
- 1 Transferkanüle (Einmalkanüle, 18 Gauge, ≥ 38 mm lang)
- 1 geflügeltes Infusionsset, 25 Gauge (orange), mit 30-cm-Schlauch (maximal 0,4 ml Füllvolumen)
- 1 steriler Mull
- Verbandpflaster
- 1 Entsorgungsbehälter für scharfe und spitze Gegenstände
Einen Überblick über die Selbstverabreichung der VYVGART s.c. Injektion findest du im Video und in der Broschüre.
Im Video bzw. der Broschüre erhältst du einen Überblick zu den wichtigsten Schritten der Vorbereitung und Verabreichung der Injektion. Bitte beachte, dass das Video und die Broschüre nur der Illustration dienen. Bitte lies dir daher vor der Anwendung von VYVGART 1.000 mg Injektionslösung sorgfältig die detaillierte Beschreibung zur Anwendung in der Packungsbeilage durch.5,†
Anwendungsvideo zur Selbstverabreichung der VYVGART-Injektion
DE-ESC-24-00010
Welche Nebenwirkungen können unter der VYVGART s.c. Fertigspritze, der VYVGART s.c. Injektionslösung sowie der VYVGART i.v. Infusion auftreten?
Die meisten davon waren in klinischen Studien mild bis moderat ausgeprägt.4,5,6
Nebenwirkungen unter VYVGART s.c. Fertigspritze sowie der VYVGART s.c. Injektionslösung:4,5
- Sehr häufig (kann mehr als 1 von 10 Behandelten betreffen) sind: Infektionen der Nase und des Rachens (Infektionen der oberen Atemwege), Reaktionen an der Injektionsstelle, darunter Rötung, Juckreiz und Schmerzen. Reaktionen an der Injektionsstelle sind normalerweise leicht bis mittelstark und treten normalerweise innerhalb eines Tages nach der Injektion auf.
- Häufig (kann bis zu 1 von 10 Behandelten betreffen) sind: Schmerzen oder Brennen beim Wasserlassen, was ein Anzeichen für eine Harnwegsinfektion sein kann, Entzündung der Atemwege in der Lunge (Bronchitis), Muskelschmerzen (Myalgie), Übelkeit.
Nebenwirkungen unter VYVGART i.v.:6
- Sehr häufig (kann mehr als 1 von 10 Behandelten betreffen) sind: Infektionen der Nase und des Rachens (Infektionen der oberen Atemwege).
- Häufig (kann bis zu 1 von 10 Behandelten betreffen) sind: Schmerzen oder Brennen beim Wasserlassen, was ein Anzeichen für eine Harnwegsinfektion sein kann, Entzündung der Atemwege in der Lunge (Bronchitis), Muskelschmerzen (Myalgie), Kopfschmerzen während oder nach der Infusion von VYVGART, Übelkeit.
Wenn du selbst Nebenwirkungen feststellst, sprich mit deiner:m Ärzt:in oder dem medizinischen Fachpersonal, sie können dir bei der Linderung der Beschwerden helfen. Dies gilt auch für Nebenwirkungen, die sich von den oben genannten unterscheiden.4,5,6
Injektions-, Infusions-, und Überempfindlichkeitsreaktionen
Unter VYVGART wurden anaphylaktische Reaktionen festgestellt.4,5,6
Der erste Behandlungszyklus und die erste Anwendung des zweiten Behandlungszyklus der VYVGART s.c. Fertigspritze und der Injektionslösung müssen unter ärztlicher Aufsicht durchgeführt werden. Die Patient:innen sollten nach der Anwendung für 30 Minuten auf klinische Anzeichen und Symptome von Injektionsreaktionen überwacht werden.4,5
Bei VYVGART i.v. sollten die Patient:innen während der Gabe und eine Stunde danach auf klinische Anzeichen und Symptome von Reaktionen im Zusammenhang mit einer Infusion überwacht werden.6
Informiere sofort deine:n Ärzt:in, wenn du während oder nach der Injektion bzw. Infusion folgende Zeichen einer schwerwiegenden allergischen Reaktion feststellst: Anschwellen des Gesichts, der Lippen, des Rachens oder der Zunge, wodurch das Schlucken oder Atmen erschwert wird, Atemnot, Gefühl das Bewusstsein zu verlieren oder Hautausschlag.4,5,6
Weitere Informationen zu möglichen Nebenwirkungen findest Du in der Gebrauchsinformation der VYVGART Fertigspritze, der Injektionslösung sowie der Infusion.
Was, wenn ich eine Injektion bzw. eine Infusion verpasse?
Wenn du eine Injektion oder Infusion verpasst hast, gib deiner:m Ärzt:in Bescheid. Sie:er wird entscheiden, ob die Verabreichung nachgeholt werden soll.4,5,6
† Die Behandlung muss von einer:m Ärzt:in eingeleitet und überwacht werden, die:der Erfahrung in der Behandlung von Patient:innen mit neuromuskulären Erkrankungen hat. Der erste Behandlungszyklus und die erste Anwendung des zweiten Behandlungszyklus müssen entweder von einer:m Ärzt:in oder unter ärztlicher Aufsicht durchgeführt werden. Die erste Selbstinjektion muss immer unter ärztlicher Aufsicht durchgeführt werden. Nach ausreichender Schulung zur subkutanen Injektionstechnik können Patient:innen oder Pflegepersonen das Arzneimittel zu Hause selbst injizieren4,5
1 Myasthenia Gravis. Rare Disease Database 2021, https://rarediseases.org/rare-diseases/myasthenia-gravis/. (abgerufen am 30.05.2024).
2 PubMed. Muscle autoantibodies in myasthenia gravis: beyond diagnosis?, https://pubmed.ncbi.nlm.nih.gov/22882218/ (abgerufen am 09.07.2024).
3 PubMed. Safety, efficacy, and tolerability of efgartigimod in patients with generalised myasthenia gravis (ADAPT): a multicentre, randomised, placebo-controlled, phase 3 trial, https://pubmed.ncbi.nlm.nih.gov/34146511/ (abgerufen am 09.07.2024).
4 Gebrauchsinformation VYVGART® 1 000 mg Injektionslösung in einer Fertigspritze, aktueller Stand.
5 Gebrauchsinformation VYVGART® 1 000 mg Injektionslösung, aktueller Stand.
6 Gebrauchsinformation VYVGART® 20 mg/ml Konzentrat zur Herstellung einer Infusionslösung, aktueller Stand.
* ab der 6. Injektion nach ausreichender Schulung der subkutanen Injektionstechnik, die erste Selbstinjektion muss immer unter Aufsicht eines Arztes durchgeführt werden.
Gebrauchsinformation VYVGART® 1 000 mg Injektionslösung in einer Fertigspritze, https://www.patienteninfo-service.de/a-z-liste/uv/vyvgart-1-000-mg-injektionsloesung-in-einer-fertigspritze (abgerufen am 27.06.2025).
Gebrauchsinformation VYVGART® 1 000 mg Injektionslösung, https://www.patienteninfo-service.de/a-z-liste/uv/vyvgart-1-000-mg-injektionsloesung (abgerufen am 27.06.2025).
Gebrauchsinformation VYVGART® 20mg/ml Konzentrat zur Herstellung einer Infusionslösung, https://www.patienteninfo-service.de/a-z-liste/uv/vyvgart-20-mgml-konzentrat-zur-herstellung-einer-infusionsloesung (abgerufen am 27.06.2025).
Pflichtangaben DE nach § 74a AMG / Fachkurzinformation AT nach § 54 AMG
Vyvgart 20 mg/ml Konzentrat zur Herstellung einer Infusionslösung/
Vyvgart 1 000 mg Injektionslösung/ Vyvgart 1 000 mg Injektionslösung in einer Fertigspritze
▼ Dieses Arzneimittel unterliegt einer zusätzlichen Überwachung. Dies ermöglicht eine schnelle Identifizierung neuer Erkenntnisse über die Sicherheit. Angehörige von Gesundheitsberufen sind aufgefordert, jeden Verdachtsfall einer Nebenwirkung zu melden. Hinweise zur Meldung von Nebenwirkungen, siehe Abschnitt 4.8 der Fachinformation. Bezeichnung: Vyvgart 20 mg/ml Konzentrat zur Herstellung einer Infusionslösung. / Vyvgart 1 000 mg Injektionslösung. / Vyvgart 1 000 mg Injektionslösung in einer Fertigspritze. Wirkstoff: Efgartigimod alfa. Pharmakotherapeutische Gruppe: Immunsuppressiva, selektive Immunsuppressiva, ATC-Code: L04AA58. Qualitative und quantitative Zusammensetzung: Vyvgart 20 mg/ml: Jede Durchstechflasche mit 20 ml enthält 400 mg Efgartigimod alfa (20 mg/ml). Sonstige Bestandteile: Natriumdihydrogenphosphat 1 H2O, Natriummonohydrogenphosphat, Natriumchlorid, Argininhydrochlorid, Polysorbat 80 (E433), Wasser für Injektionszwecke. Jede Durchstechflasche enthält 67,2 mg Natrium. Jede Durchstechflasche enthält 4,1 mg Polysorbat 80, entsprechend 0,2 mg/ml. / Vyvgart 1 000 mg Injektionslösung: Jede Durchstechflasche enthält 1 000 mg Efgartigimod alfa in 5,6 ml (180 mg/ml). Sonstige Bestandteile: Vorhyaluronidase alfa, Histidin, Histidinhydrochlorid-Monohydrat, Methionin, Polysorbat 20 (E432), Natriumchlorid, Saccharose, Wasser für Injektionszwecke. Jede Durchstechflasche enthält weniger als 1 mmol (23 mg) Natrium. Jede Durchstechflasche enthält 2,7 mg Polysorbat 20, entsprechend 0,4 mg/ml. / Vyvgart 1 000 mg Injektionslösung in einer Fertigspritze: Jede Fertigspritze enthält 1 000 mg Efgartigimod alfa in 5 ml (200 mg/ml). Sonstige Bestandteile: Vorhyaluronidase alfa, Argininhydrochlorid, Histidin, Histidinhydrochlorid-Monohydrat, Methionin, Polysorbat 80 (E433), Natriumchlorid, Saccharose, Wasser für Injektionszwecke. Jede Fertigspritze enthält weniger als 1 mmol (23 mg) Natrium. Jede Fertigspritze enthält 2,1 mg Polysorbat 80, entsprechend 0,4 mg/ml. Anwendungsgebiete: Vyvgart 20 mg/ml: Vyvgart wird zusätzlich zur Standardtherapie zur Behandlung von erwachsenen Patienten mit generalisierter Myasthenia gravis (gMG) angewendet, die Anti-Acetylcholin-Rezeptor (AChR)-Antikörper positiv sind. / Vyvgart 1 000 mg Injektionslösung / Vyvgart 1 000 mg Injektionslösung in einer Fertigspritze: Vyvgart wird zusätzlich zur Standardtherapie zur Behandlung von erwachsenen Patienten mit generalisierter Myasthenia gravis (gMG) angewendet, die Anti-Acetylcholin-Rezeptor (AChR)-Antikörper positiv sind. Vyvgart wird als Monotherapie zur Behandlung von erwachsenen Patienten mit progredienter oder rezidivierender aktiver chronisch-entzündlicher demyelinisierender Polyneuropathie (CIDP) nach vorheriger Behandlung mit Kortikosteroiden oder Immunglobulinen angewendet. Gegenanzeigen: Überempfindlichkeit gegen den Wirkstoff oder einen der oben genannten sonstigen Bestandteile. Nebenwirkungen: Vyvgart 20 mg/ml: Sehr häufig: (≥ 1/10): Infektionen der oberen Atemwege; Häufig (≥ 1/100, < 1/10): Harnwegsinfektionen, Bronchitis, Myalgie, Kopfschmerz im Zusammenhang mit dem Verfahren, Übelkeit; Nicht bekannt: anaphylaktische Reaktion während oder nach der Infusion. / Vyvgart 1 000 mg Injektionslösung: Sehr häufig: (≥ 1/10): Infektionen der oberen Atemwege, Reaktionen an der Injektionsstelle; Häufig (≥ 1/100, < 1/10): Harnwegsinfektionen, Bronchitis, Myalgie, Übelkeit. / Vyvgart 1 000 mg Injektionslösung in einer Fertigspritze: Sehr häufig: (≥ 1/10): Infektionen der oberen Atemwege, Reaktionen an der Injektionsstelle; Häufig (≥ 1/100, < 1/10): Harnwegsinfektionen, Bronchitis, Myalgie, Übelkeit. Warnhinweise: Arzneimittel für Kinder unzugänglich aufbewahren. AT: rezept- und apothekenpflichtig, wiederholte Abgabe verboten. DE: verschreibungspflichtig. Weitere Informationen, wie Angaben zu Nebenwirkungen, Schwangerschaft und Stillzeit, Warnhinweisen und Vorsichtsmaßnahmen für die Anwendung, Wechselwirkungen mit anderen Arzneimitteln und sonstigen Wechselwirkungen sind der veröffentlichten Fachinformation zu entnehmen. Pharmazeutischer Unternehmer/ Inhaber der Zulassung: argenx BV, Industriepark-Zwijnaarde 7, 9052 Gent, Belgien. Stand: Juni 2025.
DE-VYV-25-00038
Hinweis: Aus rechtlichen Gründen dürfen Informationen zu verschreibungspflichtigen Medikamenten nur medizinischen Fachkreisen oder Patient*innen mit einer Verschreibung für dieses Medikament zugänglich gemacht werden. Bei Fragen zu Therapien wenden Sie sich bitte an Ihre Ärztin bzw. Ihren Arzt.
Da Sie keine Verschreibung für dieses Medikament haben und auch nicht den medizinischen Fachkreisen angehören, sind wir aus rechtlichen Gründen nicht befugt, Ihnen Informationen bereitzustellen. Sollten Sie Fragen zu Therapien haben, empfehlen wir Ihnen, sich an Ihre Ärztin bzw. Ihren Arzt zu wenden.